
Voyages, migrants
Dengue : le développement des vaccins
La dengue est actuellement l’infection virale transmise par les moustiques la plus fréquente dans le monde. L’incidence a fortement augmenté durant ces dernières décennies. La maladie est actuellement en pleine expansion dans de nombreuses régions tropicales et subtropicales, ainsi que parmi les voyageurs qui séjournent dans ces régions.
Il existe actuellement un vaccin, qui ne peut être utilisé que dans des zones endémiques et qui n’est pas indiqué pour les voyageurs. Mais de nombreux nouveaux vaccins sont en cours de développement.
Généralités
La dengue (comme le chikungunya) est une infection virale transmise par des moustiques Aedes qui piquent durant la journée : l’Aedes aegypti et l’ Aedes albopictus (ou moustique tigre).
La dengue est transmise rarement de manière directe d’humain à humain. Il y a eu des cas sporadiques de transfert nosocomial via les muqueuses ou la peau en milieu hospitalier, de transfert périnatal, de transfert via des dérivés de sang et / ou des dons d’organes ou tissulaires.
Les virus de la dengue appartiennent au genre Flavivirus, avec quatre sérotypes qui se diffusent simultanément. Récemment, un cinquième sérotype a été découvert. Ce cinquième sérotype a un cycle "sylvatique", ce qui signifie qu’il circule principalement entre les primates non humains. À ce jour, une seule épidémie humaine causée par le sérotype 5 a été décrit (1, 2).
Immunité
- Les réponses immunitaires innées et adaptatives induites par l’infection par le virus de la dengue sont susceptibles de jouer un rôle dans l’élimination de l’infection
- L’infection par l’un des quatre sérotypes du virus de la dengue (infection primaire) assure une immunité durable contre l’infection par un virus du même sérotype. Cependant, l’immunité contre les autres sérotypes de la dengue est transitoire et les individus peuvent ensuite être infectés par un autre sérotype de la dengue (infection secondaire).
- Les anticorps contre les protéines présentes sur la surface du virus de la dengue peuvent provoquer une infection accrue des cellules portant des récepteurs d’immunoglobulines, un phénomène connu sous le nom de renforcement de l’infection par les anticorps (antibody dependent enhancement).
- La gravité de la dengue a été corrélée avec le niveau et la qualité des réponses lymphocytaires T spécifiques du virus de la dengue.
- Bien que la fièvre hémorragique liée à la dengue puisse survenir lors de l’infection par l’un des quatre sérotypes de la dengue, plusieurs études prospectives suggèrent que le risque est le plus élevé avec les virus de la dengue-2.
- Des études épidémiologiques ont montré que le risque de maladie grave est significativement plus élevé lors d’une infection secondaire par le virus de la dengue que lors d’une infection primaire.
- La dengue symptomatique due à une troisième ou quatrième infection hétérotypique après une deuxième infection est très rare. On soupçonne qu’une seconde infection (hétérotypique) renforce l’immunité non spécifique et offre une protection supplémentaire contre les sérotypes restants (immunité multitypique) (3 ; 6).
Épidémiologie
La dengue est endémique dans plus de 100 pays d’Asie du Sud, d’Amérique centrale et du Sud, du Pacifique occidental, de l’Afrique et de l’est de la Méditerranée (4, 7, 8).
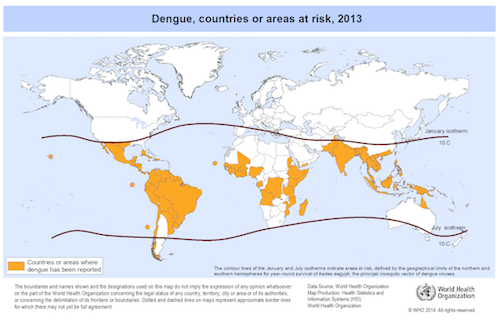
Le nombre de cas de dengue a considérablement augmenté au cours des dernières décennies. La dengue est aujourd’hui la maladie virale transmise par les moustiques dont la propagation est la plus rapide dans le monde. Au cours des 50 dernières années, l’incidence a été multipliée par 30, le virus se propageant aussi dans des pays et des régions où la maladie n’était pas présente auparavant.
Dans le monde, environ 2,5 milliards de personnes vivent dans des pays où la dengue est endémique. On estime le nombre annuel d’infections au minimum à 390 millions ; environ 100 millions de ces infections sont symptomatiques, avec plus de 3 millions de cas graves et 9.000 à 25.000 décès, principalement de jeunes enfants (7,8, 9).
L’expansion géographique de la maladie est due, entre autres, à l’augmentation de l’urbanisation, aux déplacements internationaux de personnes pendant la période d’incubation de la maladie et à la réduction de l’efficacité de la lutte contre les moustiques. Le transport international de vieux pneus, contenant de l’eau de pluie qui constitue un terrain de reproduction idéal pour les moustiques, aurait contribué de manière significative à l’extension intercontinentale (1, 3).
En Europe aussi, les vecteurs de la dengue sont présents : Aedes aegypti et Aedes albopictus (réapparition). Les données de l’ECDC (4, 7) montrent que A. aegypti est de nouveau présent à Madère après des années d’absence et peut se propager dans plusieurs pays. A. albopictus est présent dans plusieurs pays du sud de l’Europe, dont le sud de la France, l’Espagne, l’Italie, la Grèce et la Croatie.
En Belgique, sporadiquement, des moustiques et des larves d’A. albopictus ont été trouvés après l’importation de pneus usés ou de plantes de bambou, mais les moustiques ne se sont pas établis localement. La dengue reste donc une maladie d’importation.
- En 2010, il y a eu une apparition de cas autochtones en France et en Croatie, attribuée à la présence d’ A. albopictus.
- En 2012, une épidémie majeure s’est produite à Madère, au Portugal, avec plus de 2.100 cas, dont 87 touristes provenant d’autres pays.
- La France a signalé un cas indigène de dengue en 2013, quatre cas en 2014 et sept cas dans la région Provence-Alpes-Côte-d’Azur (10) en 2015.
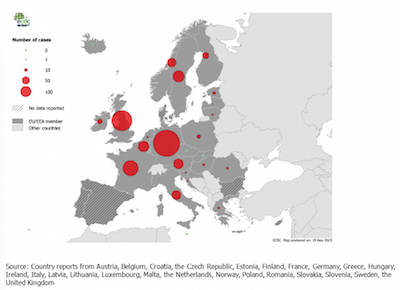
- En 2014, 1.796 cas de dengue ont été signalés pour toute l’Europe, dont 1.510 ont été confirmés. La grande majorité des cas (1.403) étaient des cas importés, quatre cas étaient autochtones ; pour 76 cas, l’origine de l’infection était inconnue. Le plus grand nombre de cas a été signalé en Allemagne (626), suivi du Royaume-Uni (376) et de la France (212). La plupart des cas sont signalés durant les mois d’été et en janvier et février, ce qui est probablement lié à des voyages à l’étranger (7).
Nombre de cas confirmés de dengue, EU/EEA, 2014
Source : ECDC. Annual epidemiological report 2015. Dengue. Stockholm : ECDC 2016.
Une étude prospective néerlandaise de 2011 portant sur 1.200 voyageurs a montré que 1,2 pour cent de ces voyageurs avaient été infectés par le virus de la dengue ; un tiers de ces infections étaient symptomatiques. L’incidence estimée était de 14,6 pour 1.000 personne/mois (1).
La dengue reste donc une maladie d’importation. En Belgique, en 2016, 117 cas de dengue ont été rapportés. Tous ces cas sont contractés à l’étranger, surtout en Asie du Sud-Est (Thaïlande et Indonésie principalement) et en Amérique (Brésil, République Dominicaine, Cuba et Costa-Rica).
Graphique : évolution annuelle des cas de dengue en Belgique
Source : Laboratoire de référence/NRC pour la dengue

Le nombre réel de cas de dengue serait en fait plusieurs fois plus élevé, car un test de laboratoire ne serait pas effectué dans tous les cas et le diagnostic ne serait pas toujours pris en considération. En outre, les voyageurs peuvent être malades pendant le voyage, en raison de la courte période d’incubation (3).
En Flandre et à Bruxelles, tout cas de dengue contracté en Europe doit être déclaré ; en Wallonie, seuls les cas autochtones doivent être déclarés.
Présentation clinique
La période d’incubation de la dengue est comprise entre 3 et 14 jours, mais le plus souvent entre 4 à 7 jours, après une piqure par un moustique infecté.
Forme asymptomatique
Environ 40 à 80% des personnes infectées n’ont aucun symptôme.
Dengue non grave ou non compliquée
La grande majorité des personnes infectées souffrent de symptômes légers. Classiquement, la dengue est décrite comme se présentant sous une forme biphasique, en pratique peu rencontrée. Dans son décours typique, la dengue se caractérise par un début brutal avec un syndrome grippal :
- fièvre (jusqu’à 41 ° C),
- céphalées (surtout région rétro-orbitale)
- douleurs osseuses et articulaires, en particulier lombosacrées
- fortes douleurs musculaires (y compris la douleur lombaire)
- douleur autour des globes oculaires
- parfois une toux sèche
- éruption cutanée.
Une amélioration clinique suit généralement, mais une aggravation peut survenir avec un exanthème maculopapulaire (morbilliforme, semblable à la rougeole) sur le corps et plus tard sur les membres et le visage. Les paumes des mains et les plantes des pieds sont généralement indemnes. La disparition de l’éruption est parfois accompagnée d’une desquamation. Un nouvel accroissement de la température peut également être concomitant de cette deuxième phase de l’éruption. La formule sanguine montre une leucopénie avec une lymphomonocytose relative, une thrombocytopénie et des tests hépatiques perturbés.
La guérison est rapide et complète dans les cas non compliqués.
La phase de récupération est cependant longue. Il peut y avoir une période prolongée de récupération difficile, caractérisée par la fatigue, des douleurs musculaires et des névralgies. Une perte de cheveux, réversible, peut parfois survenir dans les mois suivants.
Dengue grave
Rare (moins de 5%), elle peut entraîner des complications sérieuses qui mettent la vie en danger. La dengue grave commence comme une forme non compliquée, mais après 2 à 5 jours, le malade se détériore rapidement avec une tendance aux saignements (pétéchies, saignements nasaux), une réduction du volume circulant sévère avec un choc et / ou un risque de dommages graves aux organes vitaux comme le cerveau, le foie ou le cœur. En l’absence de prise en charge, la létalité est de 10%. Avec un bon traitement (correction rapide des pertes plasmatiques par perfusion), elle diminue à 1 à 2%.
L’incidence de ces formes menaçant la vie a clairement augmenté au cours des 20 dernières années.
Les facteurs de risque individuels pour un décours sérieux sont :
- la présence d’anticorps hétérologues (par infection antérieure ou présence d’anticorps maternels) ;
- l’âge : en particulier, les jeunes enfants sont moins aptes que les adultes à compenser les fuites vasculaires et présentent donc un risque accru de dengue sévère ;
- la présence éventuelle d’affections chroniques (asthme, anémie falciforme et diabète sucré).
Diagnostic (3)
Le diagnostic de la dengue se fait par détection du virus lui-même et / ou sérologie.
Dans la phase aiguë de la maladie (première semaine après le début de la fièvre), le diagnostic peut être fait avec la PCR et / ou la détection de l’antigène. L’antigène NS1 de la dengue est détectable un peu plus longtemps que l’ARN viral. La détection de l’antigène NS1 se fait également avec un test rapide, ce qui permet un diagnostic précoce. La PCR a une sensibilité et une spécificité plus élevées que la détection de l’antigène et offre l’avantage que la détermination du sérotype de la dengue est possible.
Comme les patients consultent souvent un médecin après la phase aiguë, le diagnostic nécessite généralement une sérologie. Les anticorps IgM de la dengue sont détectables à partir du cinquième à septième jour de la maladie, les anticorps IgG quelques jours plus tard. La détection des anticorps est faite avec ELISA. Certains laboratoires utilisent un test rapide IgM / IgG. Si seuls des anticorps IgM sont présents, il est conseillé de tester un échantillon de suivi une semaine plus tard pour démontrer la séroconversion des anticorps IgG, ceci en raison de résultats éventuellement faux-positifs. La sérologie présente l’inconvénient qu’une réaction croisée avec d’autres flavivirus peut se produire. Cette réaction croisée est plus prononcée avec les IgG que les IgM.
Directives pour l’échantillonnage et le transport
Un échantillon de sang d’au moins 1 ml est requis pour la sérologie et / ou la PCR. Les échantillons de sang doivent être conservés à 4 °C en attendant leur expédition. Le transport peut avoir lieu à température ambiante, sauf si l’intervalle de temps est > 24 heures (stockage à -20 °C et transport sur glace sèche). Le temps de transit doit être le plus court possible, en évitant le transport pendant le week-end ou les jours fériés.
Puisque le test effectué dépend de l’intervalle entre le début des symptômes et la collecte des échantillons, il est important de mentionner la date des premiers signes de la maladie sur le formulaire de demande.
Le Centre National de Référence (NRI) pour la dengue est situé à
Institut de médecine tropicale - Biologie clinique
Dr. M. Van Esbroeck
03 247 64 45
Traitement
Il n’y a pas de traitement antiviral spécifique de la dengue. Le plus souvent, l’infection évolue de manière spontanée vers la guérison.
Le traitement est symptomatique, avec une réhydratation en cas de fièvre. Le paracétamol peut être prescrit pour le traitement de la fièvre en cas de dengue ; par contre, l’aspirine ne doit pas être utilisée en raison d’un risque accru de saignement (11).
Dans la dengue sévère, une hospitalisation est requise pour un traitement correct (perfusions).
Prévention
Mesures de protection contre les moustiques
Les mesures de protection contre les moustiques constituent jusqu’ici la seule mesure de prévention individuelle possible. Elles doivent être appliquées dans les zones endémiques et épidémiques, de l’aube au crépuscule, en particulier en début de matinée et dans l’après-midi.
Pour les mesures anti-moustiques, voir le site de l’Institut de médecine tropicale.
Vaccination contre la dengue
Depuis des années, les chercheurs travaillent à la mise au point d’un vaccin actif contre la dengue.
La vaccination réduit le risque d’infection au niveau individuel et / ou réduit la gravité de la maladie en cas d’infection. Elle réduit aussi le risque qu’une personne infectée transmette le virus aux moustiques, ce qui réduit la pression virale et qui peut contribuer à la protection indirecte des personnes non vaccinées (6, 12).
Il existe actuellement un vaccin tétravalent atténué vivant (recombinant) contre la dengue (CYD-TDV / Dengvaxia®, Sanofi).
Cependant, le développement des vaccins contre la dengue demeure un défi majeur (13, 14, 15, 16, 17).
- Le vaccin doit fournir une protection à long terme contre les quatre sérotypes connus du virus de la dengue.
- Il ne devrait pas augmenter le risque d’infection grave chez les personnes séronégatives.
- On ne sait actuellement pas encore clairement comment la forme grave de la maladie se développe et la façon dont le virus interagit avec le système immunitaire.
- Il n’existe actuellement, pour les vaccins contre le virus de la dengue, aucune corrélation immunologique de la protection, comme la présence d’anticorps.
- Il n’existe pas non plus de modèles animaux adéquats qui peuvent prédire la protection d’un vaccin.
- Le vaccin contre la dengue ne peut être trop coûteux en raison de la survenue de la dengue principalement dans des pays pauvres.
Dengvaxia®
Dengvaxia® est indiqué pour les individus de 9 à 45 ou 60 ans (selon l’enregistrement) vivant dans la région endémique. Il est administré par voie sous-cutanée en trois doses, avec un intervalle de 6 mois (0-6-12). La durée de protection du vaccin n’est pas encore connue.
Cette vaccination n’est pas indiquée pour les voyageurs en raison de l’efficacité limitée et de l’absence de rappels naturels (11).
Dengvaxia® a jusqu’à présent été enregistré dans dix-neuf pays. Il est actuellement disponible au Mexique, en Indonésie, en Thaïlande, au Paraguay, au Pérou, au Costa Rica, au Salvador et au Guatemala. Dans deux pays, le Brésil et les Philippines, il est utilisé dans les programmes de vaccination dans les zones d’endémie pour les enfants à partir de 9 ans. Depuis lors, près de 734.000 enfants ont été vaccinés aux Philippines. En décembre 2017, toutefois, le gouvernement philippin a décidé de suspendre ce programme après avoir signalé des effets indésirables graves chez des personnes n’ayant pas été infectées par la dengue avant la vaccination (voir « Innocuité » ci-dessous).
Efficacité
Sur base de plusieurs études de phase 3 (18, 19, 20, 21) chez plus de 35.000 enfants âgés de 2 à 14 ans ou de 9 à 16 ans dans 10 zones endémiques en Asie et en Amérique latine, l’efficacité de Dengvaxia® est de 60,3% contre les infections virologiquement confirmées au cours des 25 mois suivant la première dose.
- La réduction de la dengue symptomatique était en moyenne de 57 à 65,6%.
- Le nombre de cas graves de dengue a diminué de 79,1% dans tous les groupes d’âge et de 93,2% dans le groupe d’âge de 9 ans et plus.
- Le nombre d’hospitalisations a diminué de 72,7% dans tous les groupes d’âge et de 80,8% dans le groupe d’âge de 9 ans et plus.
L’efficacité du vaccin varie selon le pays, le sérotype, la gravité de l’infection, les expositions antérieures à la dengue et l’âge.
- Pays : de 79% en Malaisie à 31,3% au Mexique.
- Sérotype. Le vaccin offre une meilleure protection contre les sérotypes DENV-3 (71,6%) et DENV-4 (76,9%) que contre les sérotypes DENV-1 (54,7%) et DENV-2 (43%).
- Exposition à la dengue. L’efficacité est beaucoup plus élevée chez les sujets séropositifs (81,9%) que chez les sujets séronégatifs (52,5%). Les patients séropositifs ont des titres d’anticorps jusqu’à dix fois plus élevés après chaque dose de vaccin que les patients séronégatifs, chez lesquels le titre d’anticorps diminue plus rapidement. Cela suggère que le vaccin contribue plutôt à renforcer l’immunité pré-existante qu’à augmenter l’immunité de protection de novo (12).
- Âge. L’efficacité du vaccin augmente avec l’âge : 66% pour les enfants de plus de 9 ans, 45% pour les enfants de moins de 9 ans et 33,7% pour les enfants de 2 à 5 ans. Cela s’explique peut-être par le fait que de nombreux enfants plus jeunes étaient séronégatifs au moment de la vaccination. D’autres facteurs possibles incluent la sensibilité spécifique à l’âge et la diminution progressive de la protection (waning).
Sécurité et limites
- Les réactions indésirables au vaccin sont similaires aux effets secondaires d’autres vaccins vivants atténués.
Les effets secondaires les plus fréquents sont : maux de tête (> 50%), malaise (> 40%), myalgie (> 40%) et fièvre (5-16%). Les réactions locales (surtout la douleur) se sont produites chez 45 à 49% des participants (9). - La vaccination pourrait fonctionner comme une infection naturelle silencieuse qui amène les personnes séronégatives, lors de la première exposition au virus naturel, à subir en fait une réinfection ou infection secondaire (12, 21).
Lors de la vaccination de routine des individus séronégatifs, le risque d’infection grave et d’hospitalisation augmente avec une nouvelle infection. A partir des nouvelles données du producteur Sanofi après cinq ans de suivi, ce risque est estimé à 2 cas supplémentaires pour 1.000 personnes n’ayant pas été préalablement infectées. C’est pourquoi Sanofi a décidé d’adapter la notice du vaccin. L’administration du vaccin n’est pas recommandée chez les personnes qui n’ont pas eu d’infection prouvée par la dengue auparavant.
Dans un avis préliminaire - dans l’attente d’un examen complet des nouvelles données d’innocuité - l’Organisation mondiale de la santé recommande que Dengvaxia® ne soit administré qu’aux personnes vivant dans des zones à forte endémie et connues pour avoir déjà été infectées par la dengue. Un nouvel avis SAGE et une publication de l’OMS sont attendus dans le courant de 2018, avec une nouvelle analyse des données de sécurité par une équipe indépendante.
Selon l’OMS, le risque est réel chez les enfants de moins de 9 ans. Par conséquent, le vaccin n’est indiqué que pour les enfants de 9 ans et plus.
Sur la base des études actuelles, ce risque est très faible chez les enfants plus âgés, en particulier dans les zones à forte endémie. Dans les zones de faible endémie, cependant, il ne peut être exclu qu’une vaccination systématique puisse augmenter l’incidence des infections graves et des hospitalisations (12, 22). Selon un certain nombre d’études, il s’agit également d’un risque non négligeable dans les zones de forte endémie (24, 25, 26), mais cela est contesté (27).
La pratique de tests sérologiques avant la vaccination pourrait être une solution pour maximiser les avantages de la vaccination et en minimiser les inconvénients. De cette façon, on pourrait éviter de vacciner les enfants séronégatifs. Pour les personnes séropositives, une dose de vaccin peut être suffisante pour une protection adéquate. En outre, les personnes qui ont déjà eu une infection secondaire et chez qui le risque d’avoir une nouvelle infection symptomatique est faible peuvent être exclues (12, 28, 29). Mais en pratique, les tests disponibles sont coûteux et la logistique de cette stratégie est très difficile (27).
Position de l’OMS
Le Groupe consultatif de l’OMS Strategic Advisory Group of Experts on Immunization (SAGE) a publié en avril 2017 un avis motivé sur l’utilisation de CYD-TDV (9, 30, 31). Selon l’OMS, l’introduction d’un programme de vaccination pour les enfants de 9 ans dans les zones à endémie élevée (séroprévalence ≥ 70%) peut réduire de 10 à 30% le nombre de cas de dengue symptomatique et d’hospitalisation sur une période de 30 ans.
- L’utilisation de ce vaccin devrait être envisagée chez les personnes âgées de 9 à 45 ans dans les pays ou zones endémiques où, sur base des données épidémiologiques, on relève une charge élevée liée à la maladie.
- La séroprévalence doit être de 70% ou plus dans la tranche d’âge qui doit être vaccinée. La vaccination des populations ayant une séroprévalence entre 50 et 70% est acceptable, mais l’impact sera beaucoup plus faible. La vaccination n’est pas recommandée lorsque la séroprévalence est inférieure à 50% en raison du risque accru d’une forme plus grave de la maladie chez les sujets séronégatifs.
- La vaccination contre la dengue devrait faire partie d’une stratégie mondiale, comptant aussi une lutte adéquate contre les vecteurs, une forte surveillance de la dengue et un traitement approprié des patients infectés.
Nouveaux vaccins en cours de développement
Il existe actuellement plusieurs nouveaux vaccins contre la dengue en cours de développement (6, 13, 14, 15, 16, 17, 32).
Trois vaccins candidats sont actuellement en phase de développement clinique (phase 2 et 3).
Deux vaccins tétravalents vivants (recombinants) (TV003 du Butantan Institute en Thaïlande et TVD de Takeda) sont actuellement testés dans plusieurs pays (phase 3) (33, 34).
Un troisième vaccin (TV003 / TV005 de NIAD) est actuellement en phase 2 (35).
Un certain nombre d’autres vaccins utilisant différentes techniques (sous-unité recombinante, ADN plasmidique, techniques d’inactivation classiques) sont toujours en phase 1 ou en phase préclinique (pas encore testé chez l’homme).
Références
1. RIVM. Dengue Richtlijn.
2. Mustafa MS, Rasotgi V, Jain S et al. Discovery of fifth serotype of dengue virus (DENV-5) : A new public health dilemma in dengue control. Med J Armed Forces India. 2015. 71(1) : 67-70.
3. Agentschap Zorg & Gezondheid. Richtlijn Infectieziekten Vlaanderen - Dengue. Versie 2016.
4. ECDC. Factsheet about dengue fever.
5. Schwartz LM, Halloran ME, Durbin AP, Longini IM Jr. (2015) The dengue vaccine pipeline : Implications for the future of dengue control. Vaccine 33(29) : 3293–3298.
doi : 10.1016/j.vaccine.2015.05.010. pmid:25989449
6. S.B. Halstead. Identifying protective dengue vaccines : guide to mastering an empirical process. Vaccine, 31 (2013), pp. 4501-4507
7. ECDC.Dengue Fever - Annual Epidemiological Report 2016.
8. www.who.int/denguecontrol/epidemiology/en
9. WHO. Dengue vaccine : WHO Position Paper. Weekly Epidemiological Record. 30 (91) : 349-364
10. Institut de Veille Sanitaire
11. Itg. www.itg.be/Files/docs/Reisgeneeskunde/Ndengue-chik.pdf
12. Ferguson NM, Rodriguez-Barraquer I, Dorigatti I, Mier YT-RL, Laydon DJ, et al. Benefits and risks of the Sanofi-Pasteur dengue vaccine : Modeling optimal deployment. Science. 2016 ; 353 (6303) : 1033–1036. doi : 10.1126/science.aaf9590. pmid:27701113
13. www.who.int/immunization/research/development/dengue_vaccines/en/
14. Vaccine Special Issue : The development of dengue vaccines. Vaccine 2011. 29 (42) : 7219-7284.
15. Vannice KS, Durbin A & Hombach J. Status of vaccine research and development of vaccines for dengue. Vaccine. 2016. 34(26) : 2934-2938. https://doi.org/10.1016/j.vaccine.2015.12.073
16. Ramakrishan L, Pillai MR & Nair RR. Dengue vaccine development : strategies and challenges. Viral Immunol. 2015. 28(2):76-84. doi : 10.1089/vim.2014.0093.
17. Betancourt-Cravioto M, Falcón-Lezama JA & Tapia-Conyer R. Roadmap for the Introduction of a New Dengue Vaccine. In : Sperança MA (ed). Dengue - Immunpathology and Control Strategies. Intech 2017. Ch 8.
18. Capeding MR, Tran NH, Hadinegoro SR et al. Clinical efficacy and safety of a novel tetravalent dengue vaccine in healthy children in Asia : a phase 3, randomised, observer-masked, placebo-controlled trial. Lancet 2014. 384(9951) : 1358-1365. DOI : http://dx.doi.org/10.1016/S0140-6736(14)61060-6
19. Villar L, Dayan GH, Arredondo-García JL et al. Efficacy of a Tetravalent Dengue Vaccine in Children in Latin America. N Engl J Med. 2015. 372 (2) : 113-123.
20. Hadinegoro SR, J.L. Arredondo-García JL, M.R. Capeding MR et al. Efficacy and Long-Term Safety of a Dengue Vaccine in Regions of Endemic Disease. N Engl j Med. 2015. 373 (13) : 1195-1206
21. Coudeville L, Baurin N, L’Azou M, et al. Potential impact of dengue vaccination : insights from two large-scale phase III trials with a tetravalent dengue vaccine. Vaccine. 2016. 34 (50) : 6426–6435. DOI:10.1016/j.vaccine.2016.08.050
22. Flasche S, Jit M, Rodríguez-Barraquer I, Coudeville L, Recker M, Koelle K, et al. (2016) The long-term safety, public health impact, and cost-effectiveness of routine vaccination with a recombinant, live-attenuated dengue vaccine (Dengvaxia) : a model comparison study. PLoS Med 13(11):e1002181. doi : 10.1371/journal.pmed.1002181.
23. Halstead S. B. Protective and Immunological Behavior of Yellow Fever Dengue Chimeric Vaccine. Vaccine. 2016. 34(14), 1643–1647.
24. Aguiar M, Stollenwerk N, Halstead SB. The impact of the newly licensed dengue vaccine in endemic countries. PLoS Negl Trop Dis. 2016 ;10(12):e0005179. doi:10.1371/journal.pntd.0005179
25. Aguiar M, Stollenwerk N, Halstead SB (2016) The risks behind Dengvaxia recommendation. Lancet Infect Dis 16(8) : 882–883. doi : 10.1016/S1473-3099(16)30168-2. pmid:27477967
26. Halstead SB. Critique of World Health Organization Recommendation of a Dengue Vaccine. J Infect Dis. 2016 ; 214(12):1793-1795. https://doi.org/10.1016/j.vaccine.2015.05.010
27. Wilder-Smith A, Vannice KS, Hombach J, Farrar J, Nolan T. Population Perspectives and World Health Organization Recommendations for CYD-TDV Dengue Vaccine. J Infect Dis. 2016 ; 214(12):1796-1799 E-pub ahead of print. doi : 10.1093/infdis/jiw341. pmid:27496977
28. Aguiar M, Halstead SB, Stollenwerk N. Consider stopping dengvaxia administration without immunological screening. Expert Rev Vaccines. 2017. 16 (4) : 301-302. http://dx.doi.org/10.1080/14760584.2017.1276831
29. Deen J. The Dengue Vaccine Dilemma : Balancing the Individual and Population Risks and Benefits.PLoS Med. 2016 ; 13(11) : e1002182. doi:10.1371/journal.pmed.1002182
30. World Health Organization Strategic Advisory Group of Experts (SAGE) on Immunization. Background paper on Dengue Vaccines prepared by the SAGE working group on dengue vaccines and the WHO secretariat. 2016
31. Pang T. SAGE committee advice on dengue vaccine. Lancet Infect Dis. 2016 ; 16 : 880–882. doi : 10.1016/S1473-3099(16)30167-0. pmid:27477966
32.Dengue Vaccine Initiative
33. Sirivichayakul C, Barranco-Santana EA, Esquilin-Rivera I, Oh HM, Raanan M, et al. Safety and Immunogenicity of a Tetravalent Dengue Vaccine Candidate in Healthy Children and Adults in Dengue-Endemic Regions : A Randomized, Placebo-Controlled Phase 2 Study. J Infect Dis. 2016 ; 213(10) : 1562–1572. doi : 10.1093/infdis/jiv762. pmid:26704612
34. Whitehead SS, Durbin AP, Pierce KK et al. In a randomized trial, the live attenuated tetravalent dengue vaccine TV003 is well-tolerated and highly immunogenic in subjects with flavivirus exposure prior to vaccination. PLoS Negl Trop Dis. 2017. 11(5):e0005584. doi : 10.1371/journal.pntd.0005584.
35. Kirkpatrick BD, Durbin AP, Pierce KK et al. Robust and Balanced Immune Responses to All 4 Dengue Virus Serotypes Following Administration of a Single Dose of a Live Attenuated Tetravalent Dengue Vaccine to Healthy, Flavivirus-Naive Adults. J Infect Dis 2015. 212(5) : 702–710. doi : 10.1093/infdis/jiv082. pmid:25801652
36. http://mediaroom.sanofi.com/information-update-on-dengvaxia/
37. http://www.who.int/immunization/diseases/dengue/q_and_a_dengue_vaccine_dengvaxia/en/
Rechercher
Abonnez-vous à la newsletter
 Vax Info
Vax Info Zika : nouvel avis du CSS
Zika : nouvel avis du CSS